ד"ר תהילה קייסמן-אלבז - נוירוכירורגית אונקולוגית
רדיוכירורגיה סטריאוטקטית לגידולי מוח - תהליך הטיפול
במאמר המבוא לרדיוכירורגיה סטריאוטקטית לגידולי מוח (להלן: רדיוכירורגיה) ניתן הסבר מפורט על עקרונות הרדיוכירורגיה, יתרונותיה וחסרונותיה וסוגי הגידולים בהם מקובל לטפל בעזרתה. השלב הראשון בתהליך הטיפול ברדיוכירורגיה הוא קבלת החלטה לגבי התאמתו של מטופל להליך. החלטה זו מתקבלת על ידי הנוירוכירורג על סמך מכלול נתונים כגון סוג הגידול, מאפייניו, מצבו הבריאותי של המטופל והעדפותיו האישיות.
המאמר הנוכחי משלים את תיאור שיטת הרדיוכירורגיה. במאמר זה ניתן הסבר מפורט על שלבי התהליך לאחר הבחירה לטפל בשיטה זו, הן מבחינת הצוות הרפואי המטפל והן מבחינת המטופל. גם כאן, המטרה העיקרית הינה לתת למטופלים רקע רחב והבנה על התהליך שהם עומדים לעבור.
תכנון הטיפול הרדיוכירורגי: מהדמיה לתוכנית קרינה מפורטת
השלב הראשון בטיפול הרדיוכירורגי הינו תכנון מפורט וקפדני של תוכנית ההקרנה. מטרת התוכנית הינה לאפשר מתן קרינה אפקטיבית לאזור הגידול תוך מזעור החשיפה לקרינה של רקמת המוח הבריאה שמסביבו. הכנת תוכנית זו כוללת מספר שלבים על פי הסדר הבא:
הדמיה: בעזרת צילום תהודה מגנטית (MRI) מתקבל מידע מפורט על מיקומו, גודלו, צורתו של הגידול ויחסיותו לרקמת המוח הסובבת אותו. הדמיה זו משמשת לתחימת גבולות הגידול וזיהוי מבנים קריטיים בקרבת מקום, כגון כלי דם, עצבים ואזורי מוח חיוניים. בדיקת טומוגרפיה ממוחשבת (CT) גם היא מבוצעת כחלק מן התכנון ומהווה חלק בלתי נפרד מן היכולת ליצור תכנית מדויקת ואישית עבור כל חולה.
סימון קווי מתאר (contouring): השלב הקריטי ביותר בתכנון התוכנית הינו סימון מדויק של קו המתאר של הגידול בכל פרוסה של תמונת ההדמיה. מטרת הסימון היא יצירת מעטפת תלת-ממדית מדויקת התוחמת את הגידול (Gross Tumor Volume). לעיתים מקובל להוסיף לסימון זה גם שוליים על מנת לקחת בחשבון אי דיוקים בסימון והתפשטות גידול מיקרוסקופית בין זמן ביצוע ההדמיה לטיפול וכך מתקבל נפח היעד הקליני (Clinical Tumor Volume) לטיפול. כיום ניתן להיעזר בתוכנות מחשב לסימון ראשוני של הגידול אך עדיין נדרשת המיומנות וההבנה של הנוירוכירורג בסימון מדויק.
קביעת מנת הקרינה: בהתאם לסוג הגידול ומאפיינים נוספים נקבעים שני פרמטרים מרכזיים:
- מנת הקרינה (Radiation Dose) שתינתן לאזור הגידול – מנת הקרינה נמדדת ביחידות גריי (Gy) המתארות את כמות האנרגיה הנבלעת ליחידת מסה של רקמה ביולוגית.
- אופן מתן הטיפול – האם לממש את כל תוכנית ההקרנה בטיפול אחד או לחלקה למספר טיפולים (ראה בהמשך).
אופטימיזציה: בחירת פרמטרים אלו מהווה אופטימיזציה בין השאיפה להבטיח פגיעה אופטימלית בתאי הגידול ובין הרצון למנוע מתן מנות קרינה גבוהות מידי לרקמת מוח בריאה או לאיברים בסיכון (Organs at Risk). מנות קרינה גבוהות מידי עלולות לגרום לנזקים כגון נמק קרינתי או פגיעה נוירולוגית. ההחלטה על מנת הקרינה וחלוקת הטיפול מתקבלת תוך הסתמכות על קווים מנחים מקובלים (guidelines) המפורסמים מעת לעת על ידי ארגונים מקצועיים בינלאומיים בתחום הנוירואונקולוגיה והרדיוכירורגיה (לדוגמא: International Stereotactic Radiosurgery Society (ISRS), American Society for Radiation Oncology (ASTRO) ועוד). קווים מנחים אלו מבוססים על אנליזה של מיטב הידע הקליני שהתפרסם בספרות המקצועית המבוקרת לגבי תוצאות טיפולים רדיוכירורגיים ברחבי העולם. קיימים כמובן פרמטרים נוספים המסייעים בתכנון על מנת לדייק את הטיפול ולהגדיר טוב יותר את שדה הקרינה וישנו גם משקל רב גם לשיקול הדעת של הרופא המתכנן.
תכנון מפורט: מקווי המתאר, מנות הקרינה שהוגדרו וחסמים על איברים בסיכון מחושב שדה הקרינה התלת-ממדי בעזרת תוכנת מחשב. התוכנה מתחשבת גם ביכולות ואילוצי מכשור ההקרנה הספציפי של המוסד המטפל, בזויות ההקרנה ובמיקום הגידול ביחס למבנים בסיכון. תהליך התכנון הכולל הינו איטרטיבי ובהחלט ייתכן שלאור אילוצים אלו ישתנו החלטות לגבי מנת הקרינה וחלוקת הטיפול. בסיום התכנון מתקבלת תוכנית הקרנה מפורטת שעומדת בדרישות הקליניות שהוגדרו וניתנת למימוש במכשור ההקרנה.
אבטחת איכות (Quality assurance): התכנון המפורט הינו מאמץ משולב של מספר מומחים. בדרך כלל מקובל שלאחר שהנוירוכירורג סיים להכין את התוכנית האונקולוג הקרינתי והפיזיקאי הרפואי בוחנים היטב ובאופן בלתי תלוי את התוכנית. בדיקה זה מתקפת את מנת הקרינה שניתנה ומוודאת שהאיברים בסיכון לא נחשפים למנות קרינה גבוהות מהמותר כדי להבטיח שהתוכנית עומדת בהנחיות וקריטריוני בטיחות שנקבעו. כמו כן, מתבצעים גם תהליכי אבטחת איכות כגון כיול, בדיקת תקינות וכיוב' במכשור הקרינה לקראת ביצוע הטיפול על מנת להבטיח הדיוק, האמינות והבטיחות של הטיפול.
חלוקת הטיפול למנות (Fractions)
כאמור, אחד הפרמטרים המרכזיים בקביעת תוכנית הטיפול הינו ההחלטה האם לתת את כל הקרינה במנה אחת או לחלקה למספר מנות. החלטה זו מתקבלת בהתאם למאפייני הגידול ולמנת הקרינה הכוללת הנדרשת.
הגישה המקורית ברדיוכירורגיה הייתה לתת את כל מנת הקרינה בטיפול בודד (Single Fraction Radiosurgery – SRS). טיפול במנה בודדת מתאים במיוחד לגידולים או מומים ווסקולריים קטנים עד בינוניים. היתרון הגדול של גישה זו הינו היכולת להשלים את תוכנית הקרינה בטיפול אחד, מה שהופך את הטיפול לנוח מאוד עבור המטופלים ומצמצם את העומס על מכון הקרינה.
מאידך, עבור גידולים בינוניים וגדולים, גידולים הממוקמים ליד איברים בסיכון, במקרה שיש מספר רב של מוקדים לטיפול (במקרה של גרורות) ובמקרה של טיפול חוזר המצב שונה. במקרים אלו, מנת הקרינה הדרושה עלולה לגרום לנזק לרקמות בריאות או למבנים בסיכון וכן להגדיל את הסיכון לתופעות לוואי חריפות.
במידה וטיפול בודד אינו מתאים, מקובל יותר ויותר לפצל את התוכנית למספר טיפולים – (Fractionated or Hypofractionated Radiosurgery – fSRS) – בדרך כלל 3-5 טיפולים שניתנים יום לאחר יום. היתרון בפיצול הינו בהקטנת העומס הקרינתי על רקמת המוח הבריאה והאיברים בסיכון ובכך מתקבל מיזעור לסיכוני הנזק לטווח ארוך ותופעות הלוואי. העקרון הביולוגי שבבסיס חלוקה זו הינו שתאי מוח בריאים יכולים להתאושש ולתקן את הנזק הנגרם להם על ידי הקרינה בעוד שתאי גידול אינם מתאוששים. על כן, פיצול תוכנית ההקרנה למספר טיפולים מאפשר לתת מנות קרינה גבוהות יותר לאזורי המוח הבריאים משניתן היה לתת בטיפול בודד.
במקרה של גידולים מרובים וכתלות בקצב ההקרנה של מקור הקרינה, יתכן פיצול של הטיפול על מנת שלא להאריך את משך הטיפול הבודד יתר על המידה (מעבר למספר שעות). החיסרון בפיצול הטיפול הינו בהגדלה של זמן הטיפול שהינה פחות נוחה למטופל ומעמיסה באופן ניכר על מכון הקרינה.
הטיפול הרדיוכירורגי עצמו – שלב אחר שלב
הטיפול הרדיוכירורגי עצמו מבוצע בדרך כלל במסגרת אשפוז יום במרפאות חוץ ואינו דורש שהמטופל יישאר לאשפוז בבית החולים לצורך השגחה. עם זאת, מבחינה הוליסטית, הטיפול נמשך חודשים ושנים אל תוך שלב המעקב והבקרה אחר תוצאות הטיפול. להלן שלבי הטיפול המרכזיים כפי שחווה אותם המטופל:
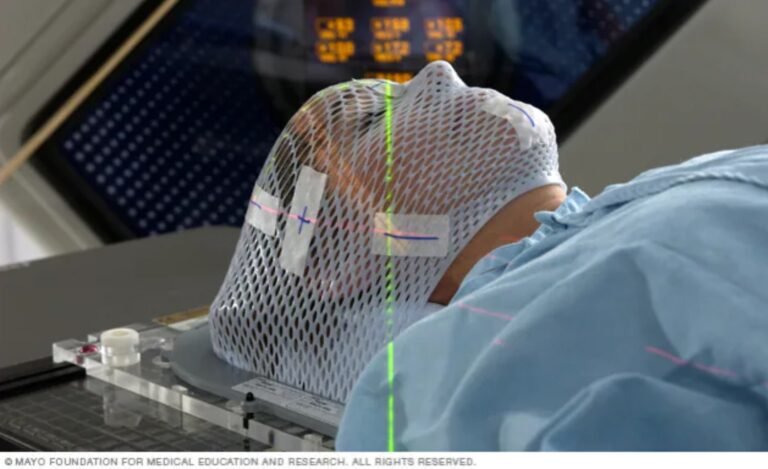
מיקום המטופל: המטופל ממוקם על שולחן הטיפולים בעזרת אמצעי קיבוע, כגון מסכה תרמופלסטית המוכנת בהתאמה אישית (ברוב המקרים) או מסגרת ראש סטריאוטקטית. מסכת ראש סטריאוטקטית תורכב במקרים מיוחדים בהם המטופל מתקשה לעבור את הטיפול באמצעות המסכה – לדוגמא כאשר המטופל קלאוסטרופובי. מטרת המסיכה הינה להבטיח התאמה מלאה בין תוכנית הקרנה שתוכננה על פי ההדמיות לבין המיקום האנטומי של הגידול במרחב וכן על מנת להבטיח תנועה מינימלית במהלך ההקרנה. אין צורך להסיר שיער מהראש כמו בניתוח. בשלב זה ייתכן ויבוצעו הדמיות נוספות על מנת לדייק ולכוונן את תוכנית ההקרנה. זהו שלב קריטי והכרחי להבטחת הצלחת הטיפול ובטיחות המטופל.
מתן הקרינה: מקור הקרינה – המאיץ הליניארי או מכונת סכין גמא מעבירים הקרינה המתוכננת מראש, למטרה בדיוק טוב ממילימטר. במהלך שלב זה, שולחן הטיפולים נע או שמקור הקרינה מסתובב סביב המטופל, בהתאם לסוג מקור הקרינה. זאת על מנת לממש את תוכנית ההקרנה על פי הזויות ומנות הקרינה שתוכננו בכל זווית בכדי להבטיח את שדה הקרינה התלת-ממדי הרצוי לטיפול בגידול. משך הטיפול אורך בין כחצי שעה עד למספר בודד שעות, בהתאם לתוכנית הטיפול שהוגדרה וקצב המנה האפשרי של מקור הקרינה (במאיץ לינארי זמני הטיפול המקובלים קצרים יותר מסכין הגמא).
חווית המטופל: מתן הקרינה מבוצע בערות מלאה. הטיפול אינו כואב אך ניתן לתת טשטוש קל או נוגדי כאבים אשר יעזרו למטופל לעבור את הטיפול בנוחות המרבית. כאשר הטיפול ניתן על ידי מכונת סכין גמא, משך הטיפול לרוב ארוך יותר ביחס לטיפול במאיץ ליניארי ולעיתים דורש הרדמה כללית של המטופל. ניתן, ואף מומלץ לשמוע מוזיקה מרגיעה או פודקאסט תוך כדי הטיפול במידה והמטופל מעוניין בכך.
ניטור במהלך מתן הקרינה: לאורך הטיפול, מיקום ראש המטופל מנוטר באופן רציף באמצעות טכניקות הדמיה שונות, כגון הדמיה סטריאוסקופית בקרני רנטגן או ניטור אופטי המבוסס על המסכה המורכבת על פני המטופל. ניטור זה, המבוצע בזמן אמת (Intrafraction), מאפשר לזהות ולתקן כל חריגה מהטיפול המתוכנן, מבטיח דיוק מירבי במתן הקרינה ומאפשר, במקרים קיצוניים, לעצור את הטיפול אם החריגה מהתכנון גדולה מהמותר.
סיום הטיפול: לאחר השלמת הטיפול, המטופל נשאר להתאוששות והשגחה לזמן קצר על מנת לנטר את תופעות הלוואי המיידיות העלולות להתרחש. הצוות הרפואי מספק למטופל הנחיות ספציפיות לגבי הטיפול הנדרש בתופעות הלוואי הצפויות ולגבי אמצעי זהירות במידה ונדרש.
שחרור: ברוב המוחלט של המקרים, המטופל יכול לחזור לביתו באותו היום שבו מתבצע הטיפול. בדרך כלל ניתן אף לחזור לפעילות היומיומית הרגילה מיד לאחר הטיפול, אך מומלץ לנקוט במשנה זהירות ביממה במהלך היממה לאחר הטיפול. ייתכנו הנחיות להימנע מפעילויות מאומצות לתקופה קצרה או לנטילת תרופות כדי להתמודד תופעות לוואי אפשריות (כגון סטרואידים ונוגדי פרכוסים).
פגישות מעקב: לאחר הטיפול נקבעת תוכנית לפגישות מעקב, הכוללת מפגשים עם הרופא המטפל. במהלך המעקב, יבוצעו סריקות הדמיה כגון MRI תקופתיות, על מנת לעקוב אחר תגובת הגידול לרדיוכירורגיה, ניטור התפתחות תופעות לוואי כלשהן ולהערכת הצלחת הטיפול. תדירות הפגישות, לפחות בשלב המיידי שלאחר הטיפול, הינן כל מספר חודשים, בהתאם למקרה הספציפי. בהתאם להצלחת הטיפול יוחלט על תוכנית המעקב ארוכת הטווח או, לעיתים, על טיפול רדיוכירורגי נוסף או טיפול אונקולוגי משלים אחר, בהתאם לסוג הגידול ולתגובתו לטיפול.
מסגרת הזמן וסימנים המעידים על הצלחת הטיפול הרדיוכירורגי
על מנת לאפשר בחינה אובייקטיבית של אפקטיביות הטיפול ולהתאים את ציפיות המטופל מהטיפול הרדיוכירורגי, מתוארים להלן מסגרת הזמן והסימנים המעידים על הצלחת טיפול. כמו בכל טיפול רפואי, מידע זה מבוסס על מידע שנאסף באופן סטטיסטי. כל מטופל מגיב אחרת לטיפול וחשוב להעריך את מצבו באופן אינדיבידואלי במסגרת תוכנית המעקב:
מסגרת זמן: השפעת הטיפול הרדיוכירורגי איננה מיידית, מכיוון שהיא תלויה בתהליכי הריפוי הטבעיים של הגוף. ההשפעות המלאות של רדיוכירורגיה עשויות לקחת שבועות, חודשים ואפילו שנים עד להערכה מלאה של הצלחת הטיפול. מסגרת הזמן המדויקת תלויה בגורמים כמו סוג הגידול, גודלו, תוכנית ההקרנה שנבחרה ומצבו הבריאותי של המטופל:
- עבור גידולים ומצבים שפירים כמו שוואנומות ווסטיבולריות, מנינגיומות ומומים ווסקולריים, עשויים לחלוף מספר חודשים עד מספר שנים עד שניתן לראות את ההשפעה המלאה של הרדיוכירורגיה.
- עבור גידולים ממאירים, כגון גרורות, תגובת הטיפול עשויה להיות מהירה יותר ובדרך כלל נהוג לראות שיפור ברור תוך שבועות או חודשים.
סימנים מעידים להצלחה: ניתן להעריך את הצלחת הטיפול ברדיוכירורגיה באמצעות גורמים שונים, ביניהם:
- תגובה רדיולוגית: מעקב אחר סריקות הדמיה מאפשר בחינה אובייקטיבית של גודל, נפח ומבנה הגידול לאורך זמן. טיפול מוצלח מוביל לשליטה בגידול – התייצבות או הפחתה בגודל או בנפח הגידול, ומניעת המשך התפתחותו ולאורך זמן גם מניעת הישנותו (Recurrence).
- הקלה בתסמינים: שיפור או העלמות תסמינים הקשורים באופן ישיר להשפעת הגידול על הרקמה הסובבת אותו (כגון הקלה משמעותית בעוצמת הכאבים הנגרמים מנוכחות גרורות בעמוד השדרה לאחר הטיפול ברדיוכירורגיה או שיפור בחסרים נוירולוגיים שהיו טרם הטיפול) מהווים אינדיקציה לטיפול מוצלח והשגת המטרה. יש לזכור שמסגרת הזמן להקלה בתסמינים משתנה בהתאם למצב בריאותו של המטופל וגורמים נוספים.
- שימור התפקוד הנוירולוגי: שימור או שיפור התפקוד הנוירולוגי בעקבות הטיפול יכולה להוות סימן להצלחת הטיפול הרדיוכירורגי.
סיכום
רדיוכירורגיה סטריאוטקטית היא שיטת טיפול לא פולשנית ויעילה לטיפול בסוגים מסוימים של גידולי מוח ועמוד שדרה ויעילה מאד גם עבור מצבים רפואיים נוספים. הכרת תהליך הטיפול, משלב ההכנה, התכנון, דרך ביצועו ועד למעקב ארוך הטווח, מאפשרת למטופל להיערך טוב יותר לטיפול, להיות מעורב בהתאמת הטיפול לצרכיו ולהתאים את ציפיותיו מן הטיפול.
למידע נוסף ומפורט יותר ניתן להקשיב לראיון שלי אצל ד"ר קרן גונן מעמותת עיל"מ (עמותה ישראלית לגידולי מוח) בנושא רדיוכירורגיה סטריאוטקטית לגידולי מוח.